Dois parâmetros que saltam aos olhos, a cor e a turbidez são dois indicadores da qualidade da água que às vezes estão interrelacionados.
A cor é geralmente um indicador da presença de metais (Fe, Mn), húmus (matéria orgânica oriunda da degradação de matéria de origem vegetal), plâncton (conjunto de plantas e animais microscópicos em suspensão nas águas) dentre outras substâncias dissolvidas na água.
A determinação de cor comumente é feita pela comparação visual com soluções de cloroplatinato de cobalto ou com discos de cor semelhantes à coloração das soluções de cloroplatinato de cobalto. É recomendável que seja feita no momento da coleta, evitando a estocagem o que poderia ocasionar variações no pH.
Costuma-se definir cor aparente e a cor verdadeira.
A cor verdadeira se refere à determinação de cor em amostras sem turbidez (Ex: após filtração ou centrifugação).
E a cor aparente se refere à determinação de cor em amostras com turbidez (com material coloidal ou em suspensão).
A técnica de comparação com cloroplatinato é mais adequada à determinação de cor de águas de fontes naturais, mas não costuma ser adequada à determinação da cor de efluentes. Nesses casos é possível variar a relação entre cloro e platina para ajustar a tonalidade da solução mas quando isso não é possivel recomenda-se o uso de técnicas instumentais (espectrofotometria).
Ao se comparar a eficiência de diferentes tratamentos para a remoção de cor, deve-se respeitar a incerteza associada a cada faixa de leitura (Tabela 3, “Incerteza associada a cada faixa de leitura de cor.(Fonte: Standard Methods for the Examination of Water and Wastewater, 20th Edition)”) e verificar o pH das amostras.
Tabela 3. Incerteza associada a cada faixa de leitura de cor.(Fonte: Standard Methods for the Examination of Water and Wastewater, 20th Edition)
A turbidez é uma medida do espalhamento de luz produzido pela presença de partículas coloidais ou em suspensão e é expressa como unidade nefelométrica de turbidez (NTU - Nephelometric Turbidity Unity) usando-se como padrão para calibração do turbidímetro uma suspensão de polímero formazin (sulfato de hidrazina + hexametileno tetramina) ou uma suspensão de látex ou então micro esferas de estireno-divinilbenzeno, conforme o fabricante do equipamento.
A turbidez é um parâmetro indicador da possível presença de argila, silt, substâncias orgânicas (Ex: húmus) ou inorgânicas (Ex: óxidos) finamente divididas, plâncton e algas. Indicando, por exemplo, o risco de entupimentos de filtros e tubulações.
Nota
Para conhecer um pouco mais o protocolo para determinação das diversas frações de partículas presentes na água veja o apêndice: Série de Sólidos.
A determinação deve ser feita o mais rápido possível evitando alterar a temperatura e o pH da amostra.
Mudanças no pH podem alterar a cor e/ou provocar a coagulação de partículas em suspensão alterando as leituras de turbidez.
Pode ser recomendável, em alguns casos, degasar a amostra para a remoção de micro bolhas de gases dissolvidos com o uso de vácuo ou ultra-som, mas com cuidado.
Ao se comparar a eficiência de diferentes tratamentos para a remoção de turbidez, deve-se respeitar a incerteza associada a cada faixa de leitura (Tabela 4, “Incerteza associada a cada faixa de leitura de turbidez.(Fonte: Standard Methods for the Examination of Water and Wastewater, 20th Edition)”)
Tabela 4. Incerteza associada a cada faixa de leitura de turbidez.(Fonte: Standard Methods for the Examination of Water and Wastewater, 20th Edition)
| Turbidez (NTU) | Incerteza |
|---|---|
| 0 - 1,0 | ± 0,05 |
| 1,0 - 10 | ± 0,1 |
| 10 - 40 | ± 1 |
| 40 - 100 | ± 5 |
| 100 - 400 | ± 10 |
| 400 - 1000 | ± 50 |
| > 1000 | ± 100 |
As substâncias responsáveis pela cor e turbidez podem, muitas vezes, se apresentar organizadas no meio aquoso em diferentes escalas de tamanho, afetando significativamente a forma como essas substâncias interagem com o solvente e os demais componentes da solução/mistura.
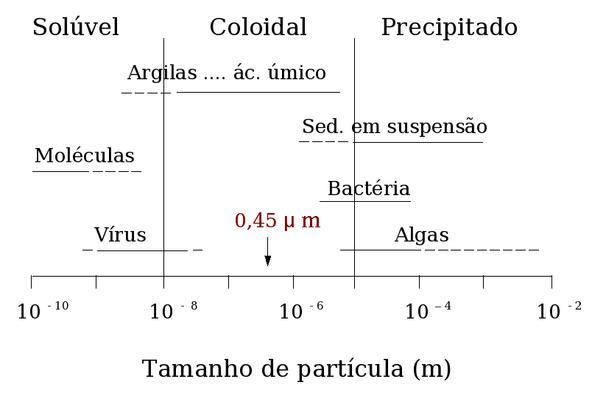
A figura seguinte ilustra a distribuição de tamanho de alguns componentes típicos de águas naturais agrupando-os em três categorias: solúvel, coloidal e precipitado.
Segundo essa classificação (arbitrária), os colóides compreendem as partículas, ou gotas, em suspensão na água com diâmetro entre ~10 nm (10-8 m) e ~10 μm (10-5 m)
Figura 2. Classificação por tamanho de materias comumente presentes em águas naturais (hidrosfera).(Environmental Chemistry - A Global Perspective
Para enterdemos o papel dos colóides em química analítica, vamos citar uma questão muito comum em Química Ambiental.
Considere o problema de analisar a concentração de fósforo em um lago para avaliar o risco potencial de eutrofização.
O fósforo pode se encontrar em 2 situações extremas: ortofosfato solúvel, disponível para as algas e plantas aquáticas e fosfato insolúvel na forma de hidróxiapatita (Ca5OH(PO4)3(s)).
Entre esses 2 extremos existe toda uma gama de material sólido com diferentes densidades e tamanhos de partícula (10nm a 10 μm), contendo compostos fosforados, orgânicos e inorgânicos.
Portanto a pergunta é: Qual a fração de fósforo total que pode ser considerada biodisponível?
Com relação à determinação de fósforo, é necessário separar a fração com o tamanho de partícula desejado. Existem técnicas de centrifugação e filtração que permitem separar as frações desejadas. Mas existe um consenso de que a filtração através de membrana com tamanho de poro de 0,45 μm permite uma separação entre a fração solúvel e insolúvel.
No entanto é importante lembrar na interpretação do resultado para a avaliação ambiental, que ao longo do tempo outras espécies contendo fósforo (biomassa ou fósforo adsorvido em partículas coloidais) maiores do que 0,45 μm, podem liberar ortofosfato solúvel para os organismos em crescimento.
As suspensões coloidais são capazes de espalhar a luz gerando o chamado efeito Tyndall, conforme ilustrado abaixo.
Por causa da sua grande área superficial, os colóides são capazes de adsorver moléculas ou íons da solução de forma reversível ou irreversível e portanto a presença de substâncias coloidais é um indicador da possível presença de outras substâncias orgânicas ou inorgânicas.
