Considerando a importância do tema Detecção para o monitoramento e/ou controle de recursos hídricos, vamos fazer uma breve introdução conceitual.
Podemos definir detecção como a ação de revelar, perceber, identificar a existência, ou medir a quantidade ou a intensidade de algo que era desconhecido, oculto.
Como estamos tratando do tema Água vamos agrupar os diferentes “parâmetros” que podem ser objetos de uma detecção em três grandes grupos:
Parâmetros Físicos - Ex: vazão, temperatura, pressão (Ver: Sensors and Transducers)
Parâmetros Químicos - Ex: concentração de cloro, nitrato, fosfato, alcalinidade
Parâmetros Microbiológicos - Ex: concentração de bactérias, protozoários
Também existem os parâmetros “Físico Químicos” que dizem respeito às propriedades físicas da água que são efeitos da composição química. Por exemplo: condutividade, pH, potencial Redox, tensão superficial, propriedades coligativas, índice de refração.
A Química Analítica é a área da Química que trata dos métodos para a determinação (detecção) da composição química, ou seja, dos parâmetros químicos.
Os métodos analíticos podem ser divididos em:
Métodos Qualitativos: fornece informações sobre a identidade das espécies atômicas ou moleculares presentes na amostra
Métodos Quantitativos: fornece informações numéricas, tais como as quantidades relativas de um ou mais componentes presentes na amostra
Fonte: (Skoog, 2002).
Os métodos analíticos geralmente são classificados como sendo clássicos ou instrumentais. Esta classificação é em grande parte histórica pois os métdos clássicos, às vezes chamados de métodos de via úmida, precederam por um século ou mais os métodos instrumentais.
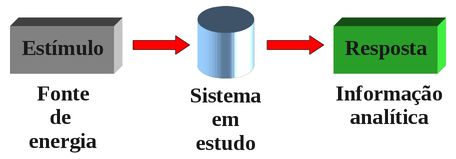
Um instrumento de análise converte a informação armazenada nas características físicas ou químicas da amostra em um tipo de informação que pode ser manipulada e interpretada. Para conseguir a informação desejada, é necessário fornecer um estímulo, que comumente tem a forma de energia eletromagnética, elétrica, mecânica ou nuclear, conforme está ilustrado na figura seguinte.
O estímulo gera uma resposta do sistema em estudo, cuja natureza e intensidade são governadas pelas leis fundamentais da física e da química. A informação obtida está associada ao fenômeno que resulta da interação do estímulo com o(s) analito(s)[6]. Um exemplo típico é a passagem de um feixe de luz visível de uma faixa estreita de comprimento de onda através de uma amostra para medir o quanto foi absorvido pelo analito. A intensidade da luz é determinada antes e depois da sua interação com a amostra, e a razão entre estas intensidades fornece uma medida da concentração do analito. (Ver a seção: Espectrofotometria)
O objetivo final em todas as medidas é que o resultado numérico obtido seja, de alguma forma, proporcional a alguma propriedade física ou química relevante do analito. E isto é feito com o uso de uma variedade ampla de dispositivos que convertem a informação de uma forma à outra.
Os termos detector, transdutor e sensor são usados frequentemente como sinônimos, mas existem algumas diferenças nos seus significados.
O mais geral dos três, o detector, refere-se a um dispositivo mecânico, elétrico ou químico que identifica, registra ou indica uma alteração em uma das variáveis na sua vizinhança, tais como pressão, temperatura, carga elétrica, radiação eletromagnética, radiação nuclear, partículas ou moléculas. Esse termo tornou-se um termo genérico aplicado também a instrumentos inteiros que frequentemente são chamados de detectores, e neste caso seria mais adequado se referir como sistema de detecção.
O termo transdutor refere-se especificamente aos dispositivos que convertem informação não-elétrica em informação elétrica e vice-versa. Por exemplo: fotodiodos, fotomultiplicadoras e outros fotodetectores eletrônicos que produzem corrente ou voltagem proporcional à potência radiante da radiação eletromagnética que incide em suas superfícies, termistores, medidores de deformação e transdutores de intensidade de campo magnético por efeito Hall.
A relação matemática entre a saída elétrica e a entrada (não-elétrica) do tipo potência radiante, temperatura, força, intensidade de campo magnético é chamada de função de transferência do transdutor.
E finalmente o termo sensor que é mais adequado para se referir à classe de dispositivos analíticos que são capazes de monitorar espécies químicas específicas de forma contínua e reversível. Por exemplo: eletrodo de vidro para pH ou eletrodos íon-seletivo, eletrodo de oxigênio de Clark.
Os sensores são formados por um transdutor acoplado à uma fase de reconhecimento quimicamente seletiva. Por exemplo, optrodos consistem de um fototransdutor acoplado a uma fibra óptica recoberta, na extremidade oposta ao transdutor, com uma substância que responde especificamente a uma característica física ou química de um analito.(Ver Sensor Óptico para Oxigênio Dissolvido (OD)