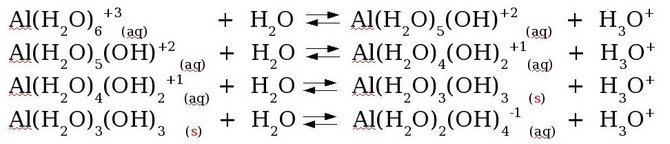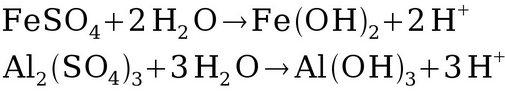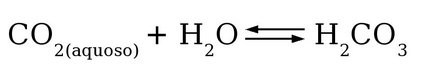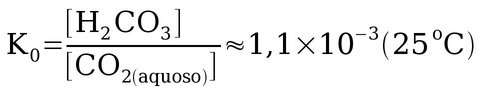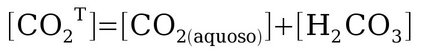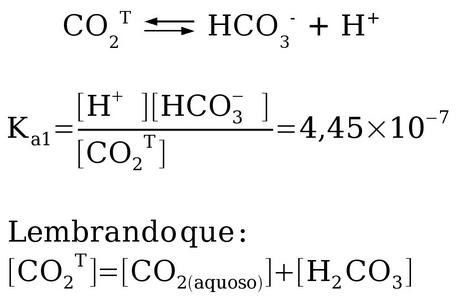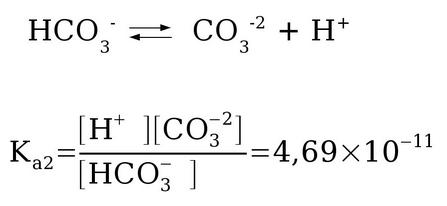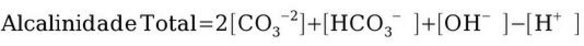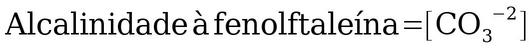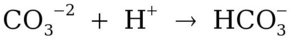Reações ácido-base em meio aquoso envolvem a troca de íons H+ entre espécies que atuam como ácido (liberando H+), outras atuando como base (recebendo H+) e a água atuando de ambas as formas.
A acidez é um parâmetro agregado, indicador da presença de ácidos minerais fortes (fosfórico, sulfídrico), fracos (H2CO3 carbônico, acético, húmicos), íons metálicos hidratados e sais hidrolizáveis (Ex: sulfato de ferro e sulfato de alumínio ).
A acidez consiste na capacidade da água em neutralizar íons OH-; é o inverso da alcalinidade que é a capacidade de neutralizar íons H+
A acidez total costuma ser determinada pela titulação da amostra até um pH determinado e portanto depende do ponto final de viragem e dos cuidados na amostragem devido a possíveis interferências devido a liberação (ou absorção) de gases dissolvidos: CO2, H2S ou NH3 devido a agitação mecânica ou variações de temperatura.
É um parâmetro expresso em mg CaCO3/L e significa a quantidade de CaCO3 necessária para neutralizar a amostra, apesar da titulação ser feita com NaOH.
O Standard Methods recomenda uma oxidação prévia da amostra com peróxido a quente no caso de amostras contendo íons metálicos hidrolisáveis.
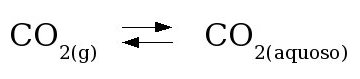
E por falar em reações ácido-base na água, vamos falar um pouco sobre o comportamento do dióxido de carbono dissolvido na água.
O CO2 e seus produtos de ionização ( HCO3- - bicarbonato e CO3-2 - carbonato) exercem grande influência nos processos químicos em meio aquoso, contribuindo significativamente para os processos corrosivos.
Uma grande parcela do CO2 encontrado na água é produzido pela degradação de matéria orgânica pelas bactérias. Até mesmo as algas produzem CO2 durante os processos metabólicos na ausência de luz.
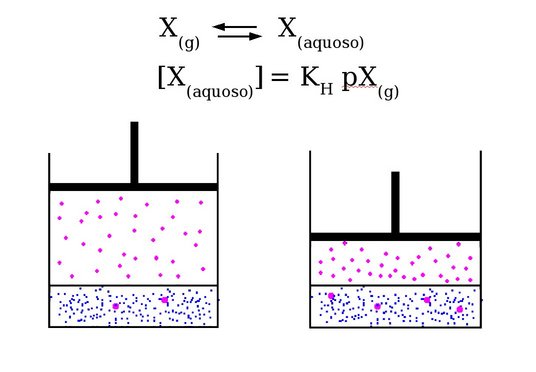
A solubilidade de gases em água é descrita pela Lei de Henry segungo a qual,em soluções ideais diluídas e a uma temperatura constante, a solubilidade de um gás em um líquido é proporcional à pressão parcial do gás em contato com o líquido.
Tabela 5. Constantes de Henry para alguns gases típicos.(Fonte: www.mpch-mainz.mpg.de/~sander/res/henry.html e Stanley E. Manaham, 2000)
| Gas | Constante de Henry a 25°C (mol x L-1 x atm-1) |
|---|---|
| O2 | 1,28 x 10-3 |
| CO2 | 3,38 x 10-2 |
| CH4 | 1,34 x 10-3 |
| N2 | 6,48 x 10-4 |
| NH4 | 1,76 x 10-2 |
Problema: Calcule a concentração (em mg/L) de CO2 dissolvido em água considerando que o ar seco é composto (em volume) por 0,037% de CO2 (ao nível do mar) e portanto a fração molar de CO2 (XCO2) no ar seco é igual a 0,00037. (Stanley E. Manaham, 2000 e Environmental Chemistry - A Global Perspective)
Dica 1: [CO2(aquoso)] = KH x pCO2
Onde
KH (cte. de Henry) = 3,38 x 10-2 mol x L-1 x atm-1 (25 °C) e pCO2 = pressão parcial de dióxido de carbono
Dica 2: A rigor, no cálculo da solubilidade de um gás em água, deve ser subtraída, da pressão atmosférica total (Po), a pressão de vapor da água (0,0313 atm a 25 °C), portanto a pressão parcial de gás carbônico é dada pela fórmula:
pCO2 = (Po - pH2O) x XCO2
A constante de equilíbro indica que a maior parte do CO2 dissolvido se encontra como CO2(aquoso) numa relação de [H2CO3] : [CO2(aquoso)] (1 : 909).
Por simplificação indicamos o CO2 dissolvido em água como CO2T.
Onde:
A formação dos produtos de dissociação do CO2 (HCO3- e CO3-2 ) contribuem significativamente para aumentar a solubilidade do CO2 na água até valores da ordem de 10 mg/L ou até maiores como no caso de águas subterrâneas.
Índice criado para representar a concentração dos ânions básicos presentes na amostra. É uma medida da capacidade da amostra se comportar como base nas reações com prótons e consiste no número de mols de H+ requeridos para titular um litro de amostra de água até atingir o ponto final.
Para soluções contendo os íons carbonato e bicarbonato a alcalinidade pode ser definida pela equação:
Contribuições menores para a alcalinidade de sistemas de água doce podem incluir amônia dissolvida e os ânions dos ácidos fosfórico, bórico e silícico. Em água subterrânea é possível a contribuição de ânions de ácidos fracos, principalmente acetato e formiato.
Águas com alta alcalinidade geralmente contêm valores altos de pH e níveis elevados de sólidos dissolvidos.
Entretanto é bom lembrar que pH é diferente de alcalinidade!
Por convenção o alaranjado de metila é o indicador usado na determinação da alcalinidade total com viragem em torno de 4,3. Sob tais condições, não apenas todo o íon carbonato foi transformado em bicarbonato, mas certamente todo o íon bicarbonato foi transformado em ácido carbônico.
Outro índice freqüentemente encontrado é a alcalinidade à fenolftaleína com viragem em torno de 8,3, onde a maior parte do íon CO3-2 foi convertido em HCO3- mas apenas uma quantidade desprezível de íon bicarbonato foi convertido em ácido carbônico. Assim,
É possível verificar essas afirmações?
Problema: Calcule o valor das razões [HCO3-]/[CO3-2] no pH de 8,3 e a relação [CO2T]/[HCO3-] no pH de 4,3.
Dica 1: 10-8,3 = 5,01 x 10-9 e 10-4,3 = 5,01 x 10-5
Dica 2: usar as equações de equilíbrio:
Figura 15. Perfil de uma Curva de Titulação. (Fonte: http://jan.ucc.nau.edu/~doetqp-p/courses/env440/env440_2/lectures/lec9/lec9.html
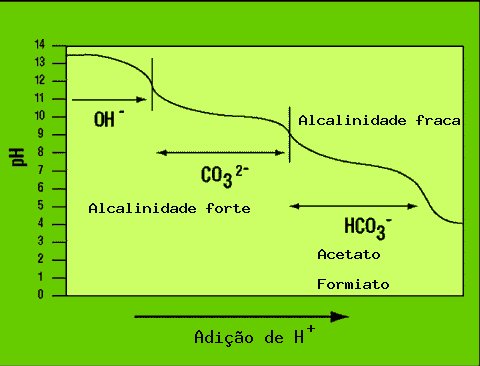
A alcalinidade pode ser determinada pela titulação com um ácido (HCl ou H2SO4 até pH 8,3 para neutralizar bases tão forte quanto ou mais fortes que o íon carbonato.
Ou pela titulação até pH 4,5 para neutralizar bases mais fracas do que o íon carbonato, mas tão fortes quanto ou mais fortes que o íon bicarbonato.
Problema: 100 mL de uma amostra de água foi titulada com 20.0 mL de HCl 0,0100M até pH = 4.3. Calcule a alcalinidade dessa amostra como mgCaCO3/l.
É importante diferenciar o significado químico da alcalinidade e do pH como indicadores das propriedades ácido-base de uma solução. O pH pode ser considerado um fator de intensidade indicando a concentração de um ácido ou uma base imediatamente disponível para uma reação de neutralização. Enquanto que a alcalinidade é um fator de capacidade que indica a capacidade de uma amostra de água em sustentar a reação com um ácido ou base adicionada.
Em resumo, a alcalinidade representa a capacidade tamponante do meio.
Note que é possível existir uma alcalinidade negativa indicando que o meio está acidificado e que portanto não restam na solução aceptores de íons H+, mas ao contrário, existe um excesso de espécies doadoras de H+.
Essa diferença pode ser ilustrada comparando uma solução 0,001 M de NaOH com uma solução 0,100 M de HCO3-. A solução de NaOH é básica (pH 11) e 1 litro dessa solução é capaz de neutralizar apenas 0,001 mol de ácido. Enquanto que a solução de bicarbonato apresenta um pH de apenas 8,3 no entanto 1 litro dessa solução é capaz de neutralizar 0,100 mol de ácido, 100 vezes mais.[1]
A alcalinidade expressa em termos de mg/l de CaCO3 se baseia na seguinte reação de neutralização:
Onde o equivalente químico do CaCO3 (50,045 g) é metade da sua fórmula grama (100,09 g).