Fontes: Handbook of Chlorination, 2010, Peterson B. Moraes, www.uniparcarbocloro.com.br.
O cloro livre é a soma das espécies que contêm átomo de cloro no estado de oxidação “0” ou “+1” e que não está combinado com amônia (NH3) ou nitrogênio orgânico.
Cloro livre (mol/L) = [Cl2] + [HOCl] + [OCl-] + [Cl3-]
Em uma solução (ácida) de cloro concentrada, preparada pela dissolução do gás cloro em água, o cloro livre estará presente quase inteiramente como Cl2 e HOCl, e talvez traços de Cl3- e praticamente nenhum OCl-.
Em soluções diluídas e com pH menos ácido o cloro residual livre estará presente majoritariamente como uma mistura de HOCl e OCl-. E portanto nessas condições o “cloro livre” corresponde à soma das concentrações de HOCl e OCl-.
Mas nas soluções alcalinas de hipoclorito estará presente somente o íon OCl-, e eventualmente algum complexo ou par iônico formado. E portanto nessas condições o “cloro livre” é igual à concentração do íon hipoclorito (OCl-).
O cloro combinado se refere ao cloro que está combinado com amônia (NH3) formando cloraminas: monocloramina (NH2Cl), dicloramina (NHCl2) e tricloramina ou tricloreto de nitrogênio (NCl3).
Conforme mostra a tabela seguinte, os átomos de cloro nas espécies de cloro que estamos considerando (HOCl, OCl-, NH2Cl, NHCl2 e NCl3) possui estado de oxidação “+1” (exceto o Cl2).
Figura F.1. Estados de oxidação de alguns compostos de cloro. (Fonte: Handbook of Chlorination, 2010)
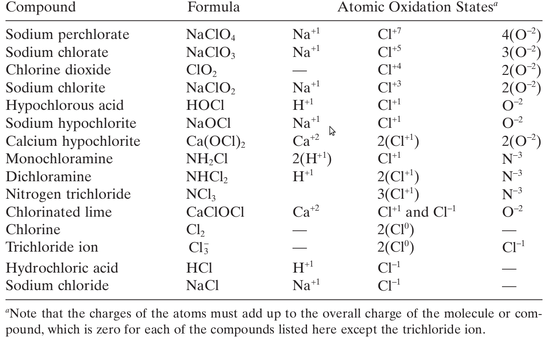
Portanto em uma reação de oxiredução cada átomo de cloro (com número de oxidação +1) é capaz de aceitar “2” elétrons para ser reduzido ao estado de oxidação termodinâmicamente mais estável do cloro (-1), o cloreto (Cl-), conforme as reações seguintes:
HOCl + 2e- → Cl- + OH-
NaOCl + 2e- + H2O → Cl- + Na+ + 2OH-
Ca(OCl)2 + 4e- + 2H2O → 2Cl- + Ca+2 + 4OH-
NH2Cl + 2e- + H2O → Cl- + NH3 + OH-
NHCl2 + 4e- + 2H2O → 2Cl- + NH3 + 2OH-
NCl3 + 6e- + 3H2O → 3Cl- + NH3 + 3OH-
Mas na molécula de cloro (Cl2) o cloro apresenta número de oxidação “0” e por isso, apesar de conter 2 átomos de cloro, aceita apenas 2 mols de elétrons na reação de redução para cloreto, pois é uma reação de desproporcionamento:
Cl2 + 2e- → 2Cl-
Portanto nas reações de oxiredução com ácido hipocloroso, hipoclorito ou monocloramina, dizemos que “1” mol do agente oxidante transfere uma quantidade de elétrons equivalente a “1” mol de Cl2.
Por isso uma solução contendo 1 mol/L de HOCl (1 Molar) é equivalente a 1 mol/L de Cl2. E se o mol de Cl2 vale 70,9g podemos expressar a concentração de HOCl em termos de Cl2 como sendo 70,9g Cl2/L ou 70900 mgCl2/L ou 70900 ppm de Cl2.
A dicloramina (NHCl2) possue 2 átomos de cloro (+1) na molécula e por isso cada mol de dicloramina aceita 4 mols de elétrons, assim como o hipoclorito de cálcio. E portanto “1” mol de dicloramina (ou hipoclorito de cálcio) possui um poder oxidante equivalente a “2” mols de Cl2.
Seguindo o mesmo raciocínio, uma solução de NHCl2 com a concentração de 1 mol/L (1 M) é equivalente a uma solução de Cl2 a 2 mol/L (2 M). E nesse caso a concentração expressa em termos de Cl2 fica 2 x 70,9 gCl2/L = 141,8 gCl2/L ou ~142000 ppm de Cl2.
Os químicos costumam usar molaridade (M) como unidade de concentração enquanto outros profissionais preferem a unidade (mg/L). Mas como os diferentes derivados clorados (NaClO, Ca(ClO)2, Cl3(NCO)3) possuem diferentes quantidades de cloro e diferentes graus de pureza se adotou como prática reportar as concentrações de cloro nos diferentes compostos derivados e nas respectivas soluções como cloro ativo ou disponível e expressar como “mgCl2/L”.
Dica
As unidades de concentração baseadas na massa do soluto pelo volume da solução (massa/volume) ou na massa do soluto pela massa do solvente (massa/massa) são muito usadas para expressar a concentrações de substâncias dissolvidas ou suspensas na água. (Unidades de concentração)
Para a maioria dos íons em água doce a unidade de concentração massa/volume mais conveniente é mg/L porque a maioria dos íons estão presentes em concentrações que vão de alguns mg/L até algumas centenas de mg/L. A unidade de concentração massa/massa equivalente é “partes por milhão” ou ppm. Por praticidade essas unidades são intercambiáveis quando se trata de água doce porque:
1mg = 10-3g e 1 litro de água ≅ 1Kg (103g) ∴
1mg da substância em 1L de água ≅ 1mg da substância/1Kg de água = 1mg da substância/106mg de água = 1 parte por milhão (ppm)
1g de soluto em 1L de água ≅ 1g de soluto/103g de água = 1 parte por mil (‰)
1g de soluto em 100ml de água ≅ 1g de soluto/100g de água = 1 parte por cem (%)
Essa equivalência só é válida se a substância dissolvida não afeta a densidade da água ou não contribui significativamente para a massa total. Caso contrário essa equivalência não é mais válida. O conteúdo salino da água do mar já é suficiente para criar uma ligeira diferença entre as concentrações expressas em mg/L e ppm, e essa diferença se torna ainda mas pronunciada em águas supersalinas. (Fonte: Water Chemistry, 2011)
Em termos práticos, cloro ativo é uma medida da capacidade oxidante de um composto ou uma solução em relação ao cloro puro (Cl2).
A rigor, cloro ativo é definido como a quantidade de iodo I2 liberado em uma solução de iodeto de potássio (KI) por uma massa do composto clorado em relação à quantidade de iodo liberado pela mesma massa de cloro gás (Cl2).
A definição se baseia na libertação de iodo, porque todas as espécies de cloro livre ou combinado podem facilmente oxidar iodeto a iodo (sob as condições ácidas utilizadas no ensaio) e, no momento em que esta terminologia foi desenvolvida, o método iodométrico era o único método comercialmente em uso.
Semi-reação do cloro: Cl20 + 2e- → 2Cl-
Semi-reação do iodeto: 2I-1 → I20 + 2e-
Oxidação do iodeto: Cl20 + 2I-1 → I20 + 2Cl-
Cada molécula de cloro (Cl2) ganha dois elétrons, formando dois íons cloreto (Cl-) enquanto que dois íons iodeto (I-1) perdem, cada qual, um elétron formando uma molécula de iodo (I2).
Nota
Em princípio a força oxidante de qualquer substância poderia ser expressa em termos de cloro ativo, mas o uso dessa terminologia é restrita a compostos oxidantes clorados.
As demais espécies de cloro reagem de forma similar:
HOCl + 2I- → I20 + Cl- + OH-
NaOCl + 2I- + H2O → I20 + Cl- + Na+ + 2OH-
Ca(OCl)2 + 4I- + 2H2O → I20 + 2Cl- + Ca+2 + 4OH-
NH2Cl + 2I- + H2O → I20 + Cl- + NH3 + OH-
NHCl2 + 4I- + 2H2O → I20 + 2Cl- + NH3 + 2OH-
Cada mol de átomos de cloro no estado de oxidação +1 irá liberar 1 mol de I2, portanto 1 mol de HOCl, OCl-, NaOCl ou NH2Cl contêm 1 mol de cloro disponível (ou ativo). O hipoclorito de cálcio e a dicloroamina contêm, cada qual, dois átomos de cloro no estado de oxidaçãp +1, por isso 1 mol desses compostos liberam 2 mols de iodo e portanto 1 mol de um desses compostos contêm 2 mols de cloro diponível. Seguindo o mesmo princípio 1 mol de tricloroamina contêm 3 mols de cloro disponível.
No final dos anos 40, um comitê da “American Water Works Association” adotou o uso dos termos “cloro residual livre disponível” e “cloro residual combinado disponível”. Mas como ambos os termos cloro livre e cloro combinado se referem a espécies que contêm cloro disponível, o termo “disponível” foi considerado redundante e saiu da terminologia padrão.
Em muitos casos um profissional precisa saber o quanto adicionar de um produto sólido ou em solução para a desinfecção de água ou de um efluente. Por exemplo qual a concentração (em %) de cloro ativo em hipoclorito de cálcio (Ca(OCl)2) com 100% de pureza?
Massa molar do (Ca(OCl)2) = 40,08 + 2x(16,00 + 35,45) = 142.98
Massa molar do Cl2 = 2x35,45 = 70,90
Cloro ativo em Ca(OCl)2 = 2 mols de Cl2 por mol de Ca(OCl)2
Porcentagem de cloro ativo = 2x70,90/142,98 = 0,9917 = 99,2%
Portanto ao adicionar 1 Kg de Ca(OCl)2 (100%) em água estamos adicionando o equivalente a 992g de cloro puro.
Um cálculo semelhante pode ser feito para determinar o teor de cloro ativo para outros compostos clorados.
Tabela F.1. Percentual de cloro ativo para alguns compostos clorados
| Composto | Massa Molar | Cloro Ativo | |
|---|---|---|---|
| mol/mol | % | ||
| Cl2 | 70,91 | 1 | 100.0 |
| HOCl | 52,46 | 1 | 135,2 |
| NaOCl | 74,44 | 1 | 95,3 |
| Ca(OCl)2 | 142,99 | 2 | 99,2 |
| NH2Cl | 51,48 | 1 | 137,7 |
| NHCl2 | 85,92 | 2 | 165,1 |
| NCl3 | 120,37 | 3 | 176,7 |
Multiplicando-se a concentração de cloro ativo pela concentração do composto em mg/L obtêm-se a concentração de Cl2 em mg/L. Por exemplo: qual a concentração de Ca(OCl)2 (com teor “comercial” de 65% de cloro ativo) necessária para uma concentração final de 4,0mgCl2/L?
mgCa(OCl)2/L x 0,65 = 4,0 mgCl2/L
mgCa(OCl)2/L = 4,0/0,65 = 6,15
Exemplo: Quantos litros de NaOCl a 10% (p/p)[32] de cloro ativo devem ser adicionados a 1 milhão de litros de água para uma concentração final de 3,0mgCl2/L?
Com 3mgCl2/L teremos 3mgCl2 em 1 litro então em 1 milhão de litros (106 L) teremos:
106 L x 3mgCl2/L = 3x106mgCl2 = 3x103gCl2
Uma solução a 10%(p/p) de cloro ativo significa 10g Cl2/100g de solução ≅ 100g Cl2/1L de solução (considerando a densidade da solução ≅ 1 Kg/L).
Portanto o volume de NaOCl a 10% que contém 3x103gCl2 é:
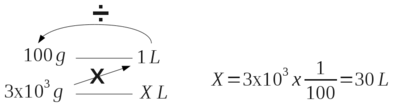
Uma outra forma de resolver é usar uma regra de três “inversa”. Seria necessário adicionar 3x103gCl2 se estivesse a 100% de pureza, mas como está com 10% de pureza temos que adicionar Xg que pode ser calculado pela seguinte regra de três inversa:
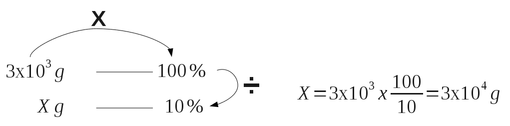
Como a densidade é ≅ 1g/mL (1Kg/L) então 30000g ≅ 30L
E finalmente o cálculo ainda ser feito com a fórmula de diluição:
Vi × Ci = Vf × Cf
Onde:
Vi - Volume inicial
Ci - Concentração inicial
Vf - Volume final
Cf- Concentração final
Uma solução a 10% de cloro ativo significa 10gCl2/100mL de solução = 100gCl2/1L de solução ou 105mgCl2/L.
Se queremos saber qual o volume (Vi) de uma solução com concentração inicial (Vi) de 105mgCl2/L que deve ser diluída para o volume final (Vf) de 106L com concentração final (Cf) de 3,0mgCl2/L, usamos a fórmula de diluição:
Vi × Ci = Vf × Cf
Vi × 105 mgCl2/L = 106 L × 3,0 mgCl2/L
Vi = 3 × 106 / 105
Vi = 30 L
[32] A Anvisa (Agência Nacional de Vigilância Sanitária) define “Água Sanitária” como sendo “solução aquosa à base de hipoclorito de sódio ou cálcio, com teor de cloro ativo entre 2,0 a 2,5% p/p (percentual em massa), durante o prazo de validade máximo de 6 meses”. (Fontes: http://www.inmetro.gov.br/consumidor/produtos/agua_sanitaria_2014.pdf e http://www.ceompf.com.br/arq/20120229145742575872724.pdf)