Organizamos neste apêndice algumas informações básicas sobre “Espectrofotometira de Absorção”.
A ligação entre luz, eletricidade e magnetismo foi sendo concebida ao longo do tempo através de sucessivas descobertas.
O astrônomo William Herschel, investigando a relação entre luz e calor utilizando um termômetro e um prisma, descobriu que a temperatura era maior em uma região além da região do vermelho no espectro de cores da luz visível. Herschel sugeriu que deveria haver "algum tipo de luz" que não era perceptível ao olho humano.
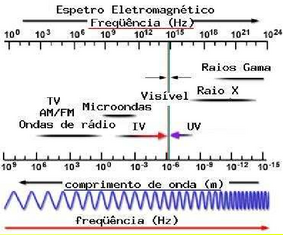
O termo, radiação eletromagnética, proposto por James Clerk Maxwell, designa as características elétricas e magnéticas características a todas as formas de enegia ondulatória da qual a luz visível representa apenas uma pequena fração.
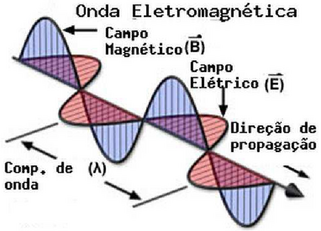
A medida padrão para o comprimento de onda (λ) costuma ser feita em nanômetro (10-9 m) e definida como a distância entre dois picos (ou vales) sucessivos.
A frequência (f) corresponde ao número de ciclos (comprimentos de onda) que passam por um dado ponto por segundo e expressa comumente em Hz ou cps (ciclos por segundo).
Essas grandezas estão relacionadas entre si e com a velocidade da luz (c) pela seguinte relação: c = λ x f
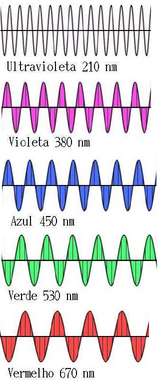
A cor é relacionada com os diferentes comprimento de onda do espectro eletromagnético. (Fonte: Wikipedia)
Tabela J.1. Faixas do Espectro Visível
| Comprimento de Onda (nm) | Cor |
|---|---|
| 340-400 | Ultravioleta próximo (Invisível) |
| 400-430 | Violeta |
| 430-500 | Azul |
| 500-570 | Verde |
| 570-620 | Amarelo - Laranja |
| 620-670 | Vermelho claro |
| 670-750 | Vermelho escuro |
| 750 | Infravermelho próximo (Invisível) |
J.1.4. Absorção da Radiação (Fonte: Skoog, 2002)
Quando uma radiação eletromagnética atravessa uma camada de um sólido, líquido ou gás, algumas frequências são seletivamente removidas pela absorção, um processo no qual a energia eletromagnética é transferida para átomos, íons ou moléculas que compõem a amostra.
A absorção promove essas “entidades” (átomos, íons ou moléculas) do seu estado normal à temperatura ambiente, ou estado fundamental, para um ou mais estados excitados de maior energia.
De acordo com a teoria quântica, átomos, íons ou moléculas têm somente um número limitado de níveis de energia discretos e para que a absorção da radiação ocorra, a energia do fóton de excitação deve ser exatamente igual à diferença de energia entre o estado fundamental e um estado excitado da amostra absorvedora.
Uma vez que essa diferença de energia é única para cada espécie, um estudo das frequências da radiação absorvida fornece um meio de identificar os constituintes de uma amostra de matéria. Para isso determina-se experimentalmente um gráfico da absorbância [33] em função do comprimento de onda, ou da frequência.
Figura J.4. Espectros de absorção para pigmentos vegetais (Clorofila A, Clorofila B e Carotenóides). (Fonte: www.plantingscience.org
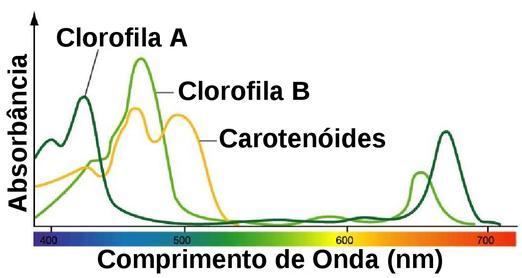
Os espectros de absorção variam muito na aparência: alguns são constituídos por numerosos picos estreitos, enquanto outros consistem de curvas contínuas e largas. Essas diferenças se devem a diversos fatores, tais como a complexidade, estado físico e vizinhança da espécie absorvedora.
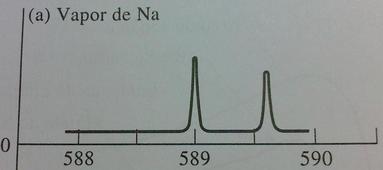
A passagem de radiação visível ou ultravioleta policromática através de um meio contendo partículas monoatômicas, como o mercúrio ou sódio gasosos, provoca a absorção de algumas frequências bem-definidas. Por exemplo, o vapor de sódio exibe dois picos de absorção estreitos e próximos na região do amarelo do espectro visível (589,0 e 589,6 nm), que são o resultado da excitação do elétron 3s para dois estados 3p que diferem ligeiramente em energia, além de várias outras linhas estreitas de absorção, que correspondem a outras transições eletrônicas permitidas.
Figura J.5. Picos de absorção do vapor de sódio em 589,0 e 589,6 nm.(Fonte: Skoog, 2002, página 132)
As radiações visível e ultravioleta têm energia suficiente para provocar transições somente dos elétrons da camada mais externa, ou dos elétrons de ligação. Por outro lado, as frequências dos Raios X são muito mais energéticas e portanto são capazes de interagir com os elétrons mais próximos do núcleo dos átomos.
É a absorção seletiva de luz visível que determina a cor exibida pela maior parte das substâncias. Quando uma amostra de matéria absorve praticamente toda a gama de radiações visíveis, não transmitindo nem refletindo luz, então ela apresenta-se-nos preta. Se, pelo contrário, praticamente nada absorve de luz visível, tudo transmitindo ou refletindo da luz incidente, então trata-se de uma substância incolor (se essencialmente transmite luz recebida) ou branca (se essencialmente a reflete). Entre estes dois casos extremos situam-se as substâncias ou materiais coloridos. A percepção de cor é o resultado da absorção seletiva de diferentes comprimentos de onda. (Fonte: http://www.angelfire.com/ab/prvs/absor.html
Figura J.6. Conjunto dos comprimentos de onda correspondentes ao espectro de emissão de uma lâmpada de tungstênio-halogênio (luz branca)(Fonte: Site da Profa. Deborah H. M. Bastos)
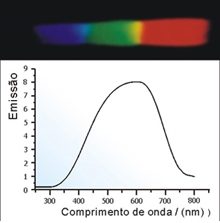
Figura J.7. Região espectral transmitida por uma solução aquosa de azul de bromotimol 10-5molar (laranja!) e o respectivo espectro de absorção.(Fonte: Site da Profa. Deborah H. M. Bastos)
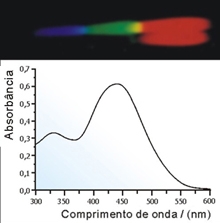
Figura J.8. Região espectral transmitida por uma solução de solução etanólica (amarela) de fluoresceína 10-5 molar e o respectivo espectro de absorção.(Fonte: Site da Profa. Deborah H. M. Bastos)
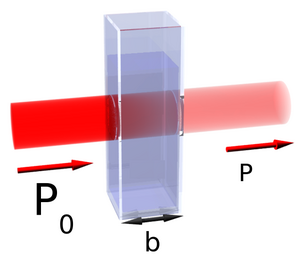
A figura abaixo mostra um feixe de radiação monocromática de Potência P0 incidindo sobre uma solução, o qual, após os processos internos de absorção sai da solução com uma potência radiante P.
Figura J.9. Diagrama da absorção de um feixe de luz "monocromática" atravessando uma cubeta de tamanho b.(Fonte: Wikipedia)
A quantidade de radiação absorvida pode ser calculada de diferentes maneiras, Transmitância ou Absorbância:
Transmitância, T = P/P0
T(%) = 100 x T
Absorbância, A = log10 P0/P
A = log10 1/T
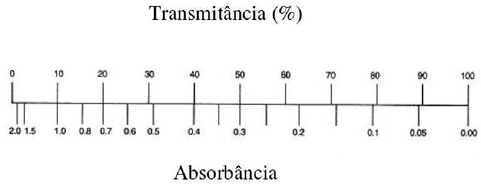
Figura J.10. Para uma solução com transmitância de 100% a Absorbância é zero e se toda a luz for absorvida a transmitância é 0 e a absorbância é infinita!
A lei de Lambert-Beer pode ser expressa pela equação:
A = ebc
A - é a absorbância (adimensional, A = log10 P0/P),
e - absortividade molar ou coeficiente de extinção molar (L mol-1 cm-1)
b - caminho óptico (cm)
c - concentração do analito na solução (mol L-1)
Atenção
Por que se usa a Absorbância ao invés da Transmitância em análises quantitativas?
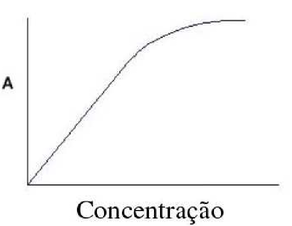
Porque, (até um limite de concentração) existe uma relação linear entre a absorbância e a concentração da substância absorvente. Portanto, mantendo-se o caminho óptico constante, pode-se determinar a concentração de uma espécie em solução, através da medida de absorbância.
Figura J.11. Gráficos da relação de Transmitância e Absorbância para diferentes concentrações de permanganato de potássio.
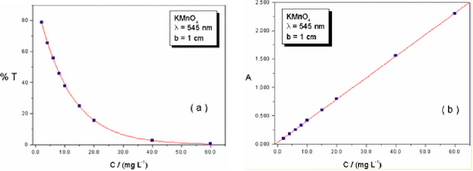
Na prática, um gráfico de calibração (absorbância versus concentração), da espécie de interesse é construída com o uso de soluções padrão (de concentração conhecida) e a concentração da amostra que se quer analisar é determinada pela interpolação da leitura de absorbância no gráfico de calibração.
No entanto a relação não é linear para altas concentrações. Por isso é importante definir a faixa de concentração adequada para medidas quantitativas, na qual a relação entre absorbância e concentração é linear.
Atenção
Por isso uma regra prática em Química Analítica é evitar fazer leituras com absorbância maior que 1, ou seja, construir a curva de calibração com valores de absorbância menor que 1.
Qual o significado de "e" na equação A = ebc ?
Rearranjando:
e = A / bc
"e" é a absortividade molar e pode ser definida como a quantidade de luz que é absorvida por unidade de concentração.
É constante para uma determinada substância.
Para se ter uma idéia, a absortividade molar dos íons Cu+2 em solução de sulfato de cobre (CuSO4) é 20 L mol-1 cm-1 enquanto o β-caroteno, responsável pela cor das cenouras, possui uma absortividade molar de 100.000 L mol-1 cm-1.
Fiz uma introdução muito sucinta da espectrofotometria de absorção molecular. Agora vamos fazer um breve resumo da instrumentação usada.
[33] Absorbância é uma medida do decréscimo na potência radiante que atravessa uma camada de um sólido, líquido ou gás.