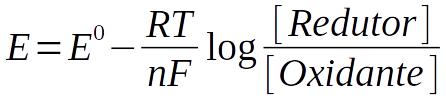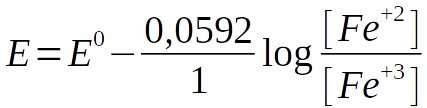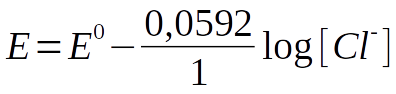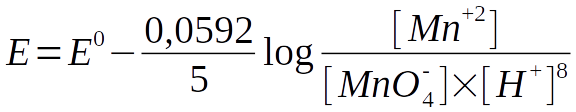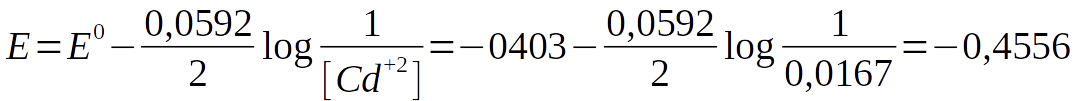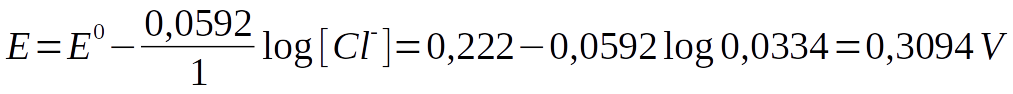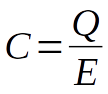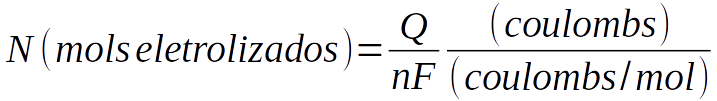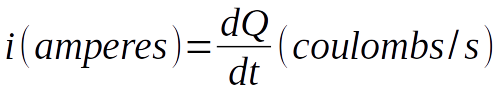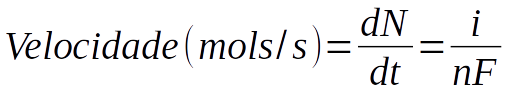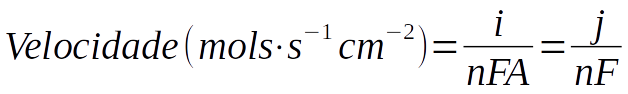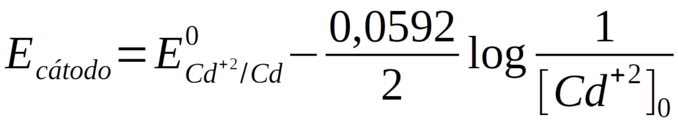Principais fontes utilizadas na elaboração dessa seção: Electrochemical Methods: Fundamentals and Applications, 2nd Edition, 2000, Skoog, 2002 e Handbook of Chlorination, 2010.
Como vimos na seção anterior, se for aplicado um potencial externo a uma célula galvânica, é possível “forçar” uma reação no sentido oposto ao sentido da reação “espontânea”. E neste caso teremos uma célula eletrolítica e não mais uma célula galvânica.
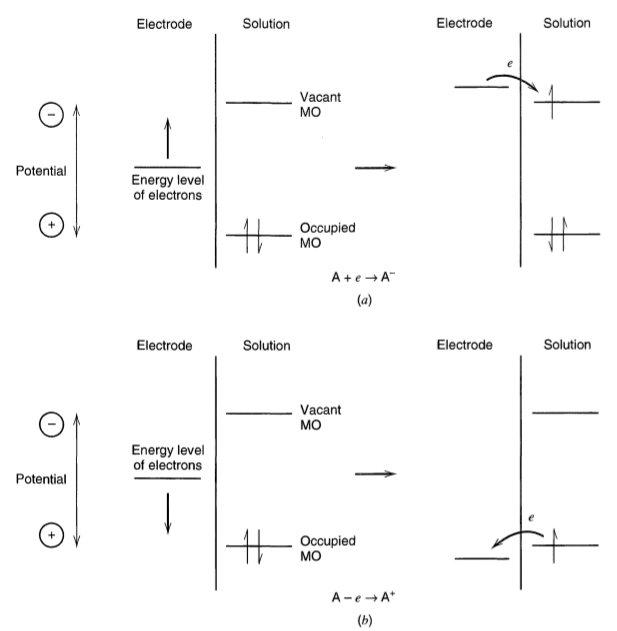
Por exemplo, a aplicação de um potencial negativo crescente a um eletrodo aumenta a energia dos elétrons até o ponto em que os elétrons são transferidos do eletrodo para um nível desocupado da espécie química em solução gerando uma corrente de redução, como mostra a figura D.8.
Por outro lado, se for aplicado ao eletrodo um potencial positivo crescente chega-se a um ponto onde os elétrons se transferem de uma espécie química na solução para o eletrodo gerando uma corrente de oxidação.
Figura D.8. Diagrama de energia da transferência de elétron em uma redução (a) e uma oxidação (b) (Fonte: Encyclopedia of Electrochemistry Vol.3 Instrumentation and Electroanalytical Chemistry, 2003)
A aplicação de um potencial “mais negativo” é feita ligando o eletrodo ao polo negativo de uma bateria ou de uma fonte elétrica de CC (corrente contínua). E nesse caso o nível de energia dos elétros no eletrodo é elevado.
Os materiais típicos dos eletrodos são os metais sólidos (Pt, Au, Ag, Cu), metais líquidos (Hg, amálgamas), carbono (grafite) e semicondutores (óxido de Sn e In, silício).
E como eletrólito temos usualmente soluções líquidas contendo especies iônicas tais como H+, Na+, Cl- em água ou solventes não aquosos. O importante é que a resistividade da solução seja suficientemente baixa (ou condutividade suficientemente alta) para permitir o processo eletrolítico.
Como visto na seção anterior, para uma reação de “redução” deve haver uma reação de “oxidação” correspondente. Mas normalmente, em uma célula eletroquímica estamos interessados em apenas uma das reações (oxidação ou redução). E o eletrodo no qual ocorre a reação de interesse é chamado de eletrodo de trabalho (ou indicador). E para observar a variação de potencial apenas nesse eletrodo pode-se “padronizar” o potencial do outro eletrodo utilizando um eletrodo de referência, no qual a composição permanece “praticamente” constante ao longo do processo (Ex: Ag/AgCl).
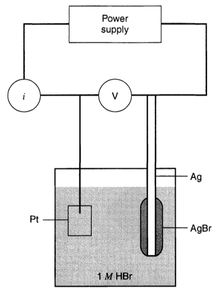
Vamos considerar um processo eletroquímico típico no qual um eletrodo de trabalho e de referência são colocados em uma solução de HBr (1 M), e nos quais é aplicada uma diferença de potencial variável, como mostra a figura D.9
Essa variação de potencial (E) pode produzir um fluxo de corrente no circuito externo devido à trasferência de elétrons entre as interfaces eletrodo|solução na medida em que as reações eletroquímicas ocorrem.
Nesse caso o número de elétrons que atravessam uma interface dependem do andamento da reação. Ou seja, existe uma relação “estequiométrica” entre o número de elétrons e o número de moles de reagentes consumidos e produtos formados na reação.
O número de elétrons é medido pela carga total (Q) (corrente × tempo - A×s) que passa pelo circuito, que é expressa em coulombs (C), onde 1 C corresponde a 6,24 × 1018 elétrons.
A relação entre a carga elétrica (Q) e a quantidade de produto formado, ou reagente consumido, é dada pela Lei de Faraday segundo a qual a passagem de 96485,33 C mol-1 corresponde a 1 “equivalente” da reação, ou seja, consumo de 1 mol de reagente, ou produção de 1 mol de produto, em uma reação de “1” elétron por mol.
Onde:
N = número de moles do reagente
Q = carga eletrica (C)
n = número de elétrons
F = constante de Faraday = 96485,33 C mol-1
Figura D.9. Diagrama de uma célula eletroquímica Pt|HBr(1 M)|AgBr|Ag ligado a uma fonte e medidores para o registro da corrente (I) em diferentes potenciais (E) aplicados (I X E) (Fonte: Encyclopedia of Electrochemistry Vol.3 Instrumentation and Electroanalytical Chemistry, 2003)
A corrente (I) é o fluxo de elétrons (ou coulombs) e 1 ampére é equivalente a 1C/s. E os gráficos da corrente (I) gerada em diferentes potenciais (E) aplicados (I X E) pode ser muito informativo sobre a natureza da solução e dos eletrodos e sobre as reações que ocorrem nas interfaces.
Os potenciais elétricos nos quais esses processos acontecem estão relacionados com os potenciais padrão de redução enquanto que a velocidade do fluxo de elétrons depende da cinética da reação.
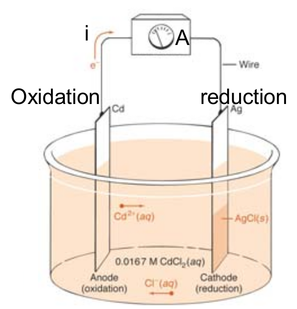
Por exemplo, a célula galvânica (Figura D.10) com um eletrodo de cádmio (Cd) e um eletrodo de prata com uma cobertura de cloreto de prata em uma solução de cloreto de cádmio (CdCl2) tende a desenvolver “espontâneamente” a reação D.15
Figura D.10. Cela galvânica contendo um eletrodo de Cd e um eletrodo de Ag recoberto com AgCl em solução de CdCl2 (0,0167 M) (Fonte: http://chem320.cs.uwindsor.ca/Notes_files/320_l13.pdf)
A reação global é o resultado da combinação da semi-reação D.16 e semi-reação D.17
Equação D.16. Semi-reação de redução do cádmio com o respectivo potencial padrão de redução (E0) (Fonte: Potencial Padrão de Eletrodo)
Cd+2 + 2e- ⇆ Cd(s) E0 = -0,403V
Equação D.17. Semi-reação de redução da prata com o respectivo potencial padrão de redução (E0) (Fonte: Potencial Padrão de Eletrodo)
AgCl(s) + e- ⇆ Ag(s) + Cl- E0 = 0,222V
Nota
A reação D.17 descreve o comportamento de um eletrodo de prata imerso em uma solução saturada em AgCl. E é a soma das duas reações que seguem:
Note o potencial padrão da redução do cádmio é menor do que o potencial padrão de redução da prata, e como os elétrons tendem a “sair” da reação de menor potencial para a reação de maior potencial, podemos deduzir que os elétrons serão liberados pelo cádmio.
Para que isso ocorra temos que inverter o sentido da semi-reação de redução do cádmio e “somar” com a semi-reação de redução da prata resultando na reação global D.15.
Nota
O “Potencial de Eletrodo” é, por definição, o “Potencial de Redução”. E o “Potencial de Oxidação” é do mesmo valor mas com o sinal oposto.
A diferença de potencial “padrão” da reação global corresponde à diferença das semi-reações padrão (0,222 V - (-0,403 V) = 0,625 V).
Nota
Podemos portanto generalizar e definir que o potencial global, ou a força eletromotriz, da célula (Ecélula) é obtido pelos potenciais das semi-reações, ou meia-célula, conforme a equação:
Ecélula = Ecátodo - Eânodo
Ou seja, no eletrodo de cádmio vamos ter uma reação de oxidação com liberação de íons Cd+2 na solução e no eletrodo de prata vamos ter uma reação de redução dos íons Ag+ sendo reduzido a prata metálica (Ag0) e liberação de íons cloreto na solução.
Mas em condições reais a diferença de potencial da cela galvânica é diferente pois o potencial de eletrodo depende das concentrações das espécies presentes “que participam das reações de oxidação e redução”.
Por exemplo, a reação Ag+ + e- ⇆ Ag(s) tem maior “tendência” de ocorrer em uma solução concentrada do íon Ag+ do que em uma solução diluída desse íon.
Consequentemente o potencial do eletrodo para essa semi-reação tende a aumentar (mais positivo) com o aumento da concentração de íons prata na solução.
Esse efeito da concentração pode ser calculado com a equação de Nernst.
A equação de Nerst é definida pela equação D.19.
Onde [Redutor] é a concentração molar da espécie redutora e [Oxidante] corresponde à concentração molar da espécie Oxidante, conforme indicado na reação D.15.
A seguir alguns exemplos de semi-reações típicas e suas correspondentes equações de Nernst:
O potencial para esse par pode ser medido com um eletrodo metálico imerso em uma solução contendo ambas as espécies de ferro. O potencial depende do logaritmo da razão entre as concentrações molares desses íons.
Não há termo para o cádmio elementar no logaritmo porque se trata de uma segunda fase pura (sólido). Assim, o potencial de eletrodo varia linearmente com o logaritmo do inverso da concentração de íons cádmio.
Essa semi-reação descreve o comportamento de um eletrodo de prata imerso em uma solução de cloreto saturada em AgCl. Para assegurar essa condição, um excesso de AgCl sólido precisa estar sempre presente.
Nessa situação, o potencial depende não apenas da concentração das espécies de manganês, como também do pH da solução.
Portanto utilizamos os valores de potencial padrão de redução e a equação de Nernst para “corrigir” o potencial gerado por uma célula galvânica considerando as concentrações dos íons que participam das reações REDOX.
Por exemplo, vamos usar agora a equação de Nernst e calcular os potenciais dos eletrodos de cádmio e de prata na cela galvânica da figura D.10) considerando a solução de cloreto de cádmio (CdCl2) na concentração de 0,0167 M.
Ag|AgCl(s),Cl-(0,0334 mol L-),Cd+2 (0,0167 mol L-)|Cd
Considerando os potenciais padrão de redução (equação D.16 e D.17):
Cd+2 + 2e- ⇆ Cd(s) E0 = -0,403V
AgCl(s) + e- ⇆ Ag(s) + Cl- E0 = 0,222V
Usando a equação de Nernst calculamos o potencial do eletrodo de cádmio:
E para o eletrodo de prata:
Agora podemos calcular o potencial global, ou a força eletromotriz, da célula (Ecélula) pela equação:
Ecélula = Ecátodo - Eânodo
Ecélula = 0,3094 - (-0,4556)
Ecélula = 0,765 V
Se colocarmos o “ponto comum” (fio preto) de um potenciômetro (multímetro) no eletrodo de cádmio e a outra ponta de prova (fio vermelho) no eletrodo de prata poderá ser medida uma tensão de ~ 0,765 V
Nota
Na prática, é necessário que o instrumento de medição seja capaz de fazer a leitura sem permitir a passagem de corrente entre os eletrodos (alta impedância) para não interferir na medição.
Para converter essa célula galvânica da figura D.10 em uma célula eletrolítica é necessário aplicar um potencial “maior” que 0,765 V“ e com polaridade oposta” para reverter o sentido da corrente e das reações de oxidação e redução, como mostra a figura D.11.
Figura D.11. Conversão da célula galvânica (Figura D.10) em célula eletrolítica pela aplicação de um potencial maior e com polaridade oposta.
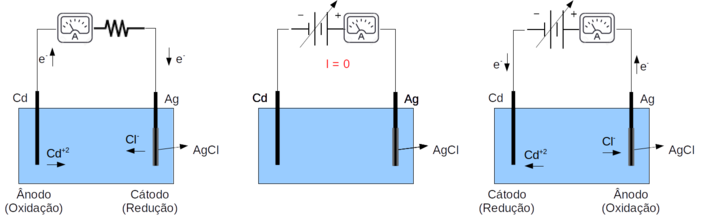
A figura D.11 mostra, de forma simplificada, as 3 situações possíveis de uma célula galvânica.
Inicialmente a cela gera um potencial “teórico” de 0,765 V, mas na prática esse potencial é menor pois com a passagem de corrente temos o efeito de “queda ôhmica” devido à resistência da solução, e de polarização, os quais serão discutidos nas próximas seções.
A figura central mostra o efeito da aplicação de um pontencial externo com polaridade oposta. Quando o potencial aplicado é igual ao potencial da cela galvânica a corrente é nula.
E a figura da direita mostra a inversão do fluxo de elétrons quando se aplica um potencial externo maior do que o potencial da cela galvânica, transformando uma célula galvânica em uma célula eletrolítica.
Nota
Lembrar que a inversão do fluxo de elétrons pela aplicação de um pontencial externo maior só ocorre quando as reações nos eletrodos são “reversíveis”.
Esses potenciais calculados são úteis mas não representam os valores obtidos experimentalmente pois se referem a células nas quais essencialmente não há passagem de corrente.
E portanto devem ser considerados fatores adicionais quando há passagem de corrente na célula.
A eletricidade é transportada dentro de uma célula pelo movimento dos íons, e assim como os condutores metálicos, as células eletroquímicas também oferecem resistência à passagem da corrente elétrica devido à resistência dos íons ao se moverem em direção ao cátodo ou ao ânodo.
Com correntes pequenas, esse comportamento segue a Lei de Ohm e podemos escrever: E = RI.
Ou seja, o produto da resistência R de uma célula em ohms (Ω) pela corrente I em ampères (A) é igual ao potencial E, chamado de “potencial ôhmico” ou “queda ôhmica”.
A resistência (R) depende dos tipos e das concentrações dos íons em solução.
O efeito da queda ôhmica é aumentar o potencial necessário para operar uma célula eletrolítica e diminuir o potencial medido de uma célula galvânica. Portanto, a queda ôhmica é sempre subtraída do potencial teórico da célula como mostra a equação D.27
Por exemplo, se a resistência interna da célula da figura D.11 for 15 Ω, qual seria o potencial necessário para se obter uma corrente de 2 mA?
Usando a equação D.27:
Ecélula = Ecátodo - Eânodo - IR
Ecélula = -0,765 - 0,002 × 15
Ecélula = -0,765 - 0,03
Ecélula = -0,795
Ou seja, para obter uma corrente de 2mA é necessário aplicar um potencial de -0,795 V
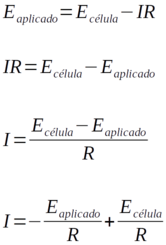
E portanto podemos reescrever a equação D.27 da seguinte forma:
Normalmente procura-se minimizar a queda IR reduzindo a resistência da célula pelo aumento da força iônica.
Um eletrodo onde NÃO há transferência de elétrons através da interface metal-solução, independente do potencial aplicado por uma fonte externa, é chamado de “eletrodo polarizado ideal” (ou eletrodo polarizável ideal).
Mas na realidade não existe um eletrodo real que se comporte dessa maneira ao longo de uma faixa ilimitada de potencial.
O que existe são alguns eletrodos que se comportam como um “eletrodo polarizado ideal” dentro de uma faixa limitada de potencial.
Por exemplo, um eletrodo de mercúrio (Hg) em contato com uma solução deaerada de cloreto de potássio (KCl) se comporta como um “eletrodo polarizado ideal” dentro da faixa de ~ +0.25 V (em relação ao eletrodo de hidrogênio padrão ou normal) até ~ -2,1 V (em relação ao eletrodo de hidrogênio padrão ou normal), ou seja em uma faixa de ~2,3 V.
Mas fora desses limites o eletrodo de mercúrio pode sofrer reações de oxiredução fugindo do comportamento ideal.
Por exemplo, em potenciais maiores do que + 0,25 V o mercúrio pode perder 1 elétron e formar o íon Hg+1 (Hg → Hg+ + e-), o qual na presença de cloreto forma o calomelano conforme a reação D.29.
Equação D.29. Equação de oxidação do mercúrio no eletrodo de calomelano saturado
Hg + Cl- → 1/2Hg2Cl2 + e-
E em potenciais mais negativos do que - 2,1V o potássio pode ser reduzido e formar um amálgama com o mercúrio metálico, segundo a reação D.30.
Portanto, nessa faixa de potencial (+0.25 V a -2,1 V) as reações de oxiredução (transferência de elétrons através da interface sólido-líquido) no eletrodo de calomelano saturado não são significativas, como mostra o gráfico da figura D.12.
Figura D.12. Gráfico de corrente X voltagem (i X E) do eletrodo de calomelano como um exemplo ilustrativo do comportamento de um “eletrodo polarizado ideal”.
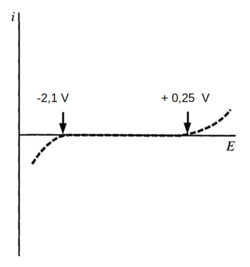
Até mesmo a eletrólise da água, apesar de ser termodinâmicamente possível em diferenças de potencial maiores do que 1,23 V, não é um processo significativo pois ocorre com velocidade muito baixa na superfície do mercúrio.
Por isso, as únicas possíveis reações de oxiredução (e correspondente corrente faradaica) são decorrentes das impurezas presentes (íons metálicos, oxigênio e moléculas orgânicas).
Como não ocorrem transferências de carga, nessa faixa de potencial, no eletrodo de calomelano a interface eletrodo solução se comporta como a placa de um capacitor devido à formação de uma dupla camada, como veremos mais adiante.
Informações sobre uma reação na superfície do eletrodo são obtidas pelo perfil da curva de corrente em função do potencial aplicado (i X E), da qual se originam alguns termos relativos aos eletrodos.
Por exemplo, se reescrevermos a equação D.28 para ter a corrente (I) como função do potencial aplicado (Eaplicado), obtemos a equação D.31.
Dessa forma, um gráfico da corrente em uma célula eletrolítica versus o potencial aplicado deve ser uma linha reta com uma inclinação igual -1/R, e interseção igual a Ecélula/R.
No entanto, experimentalmente se observa que o gráfico é linear apenas para correntes baixas, e se desvia da linearidade à medida que a voltagem aplicada aumenta, como mostra a figura D.13.
Figura D.13. Curva experimental corrente X voltagem para a operação da célula da figura D.11. A linha pontilhada representa a curva teórica considerando a inexistência de polarização. E a sobrevoltagem Π é a diferença de potencial entre as curvas teórica e a experimental.
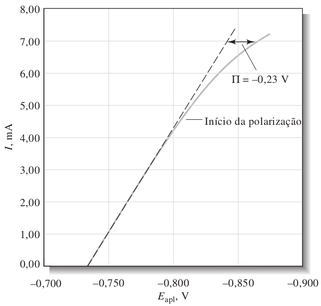
Nota
Nesse experimento, as medidas foram feitas em um tempo suficientemente curto para que nenhum dos potenciais de eletrodo variasse significativamente como conseqüência da reação eletrolítica.
Como pode ser visto na figura D.13, o gráfico é linear para correntes baixas. Mas à medida que a voltagem aplicada aumenta, a corrente finalmente começa a se desviar da linearidade. Nessas circunstâncias dizemos que a célula está “polarizada”
Nota
O termo “polarizado” é uma denominação antiga e não necessariamente a mais adequada, mas seu uso ainda está tão presente no jargão eletroquímico que é melhor manter e definir com a maior precisão possível. (Fonte: Electrochemical Methods: Fundamentals and Applications, 2nd Edition, 2000)
Portanto o termo Polarização se refere ao desvio do potencial de eletrodo do valor previsto pela equação de Nernst sob a passagem de corrente.
E o termo Sobrevoltagem (ou Sobrepotencial) se refere à diferença entre o potencial teórico da célula, segundo a equação D.28, e o potencial “real” da célula a um determinado nível de corrente.
As células que apresentam comportamentos não-lineares sob correntes elevadas exibem polarização e o grau de polarização é dado por uma sobrevoltagem, ou sobrepotencial, o qual é simbolizado por Π na figura D.13.
O efeito da polarização é aumentar o valor do potencial necessário para se obter uma corrente esperada. Por exemplo, para se obter uma corrente de 7mA na célula da figura D.11 é necessário aplicar um potencial adicional de -0,23 V.
E portanto podemos adicionar a sobrevoltagem referente à polarização na equação D.28:
A polarização é um fenômeno que pode afetar um ou os dois eletrodos em uma célula, e pode variar amplamente dependendo de fatores tais como:
tamanho, forma e composição do eletrodo;
composição da solução eletrolítica;
temperatura e velocidade de agitação;
intensidade da corrente;
estado físico da espécie envolvida na reação
Em alguns casos, se aproxima de zero, mas em outros pode ser tão grande que a corrente na célula torna-se independente do potencial. Sob essa circunstância, a polarização é considerada completa.
Fenômenos de polarização podem ser divididos em duas categorias: polarização de concentração e polarização por transferência de carga (ou cinética).
Mas afinal qual a causa dessa “Polarização”?
Primeiro vamos entender que uma célula eletroquímica é um sistema “heterogênio” composto “normalmente” por 2 fases: o eletrodo “sólido” e uma solução “líquida”.
Nesse sistema as reações eletroquímicas não ocorrem no “meio” (interior) da solução mas exclusivamente na “interface” entre o eletrodo e a solução, ou seja, na vizinhança próxima da superfície do eletrodo como mostra a figura D.14.
Figura D.14. Diagrama da estrutura heterogênia na vizinhança de um eletrodo (Fonte: Understanding electrochemistry: Some distinctive concepts, 1983)
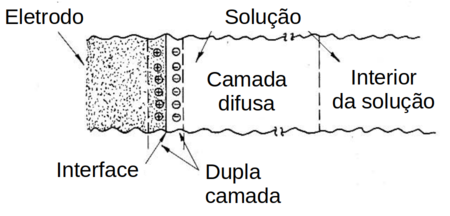
Quando se aplica um potencial a um eletrodo imerso em uma solução iônica, a passagem momentânea de corrente (eletrônica) origina um excesso (ou deficiência) de carga negativa na superfície do eletrodo. A mobilidade dos íons na solução faz a camada da solução imediatamente vizinha ao eletrodo adquirir uma carga oposta.
A camada carregada consiste em uma camada interna compacta, em que o potencial decresce linearmente com a distância ao eletrodo, e uma camada externa mais difusa, com o potencial decrescendo exponencialmente. Esse conjunto de camadas carregadas é chamado de dupla camada elétrica, como mostra a figura D.15.
Figura D.15. Dupla camada elétrica formada na superfície do eletrodo como resultado de um potencial aplicado. (Fonte: http://zeus.qui.ufmg.br/~valmir/livros/Condutometria-Otto.pdf)
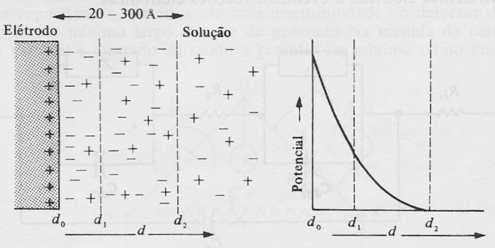
A corrente capacitiva aumenta com a intensidade do potencial aplicada e com a área do eletrodo.
Para compreender o fenômeno, imagine um elétron que se desloque de um circuito externo para a superfície do eletrodo. Quando o elétron atinge a interface da solução pode acontecer apenas dois processos. Ele pode permanecer na superfície do eletrodo e aumentar a carga na dupla camada ou se transferir para uma espécie química na solução em uma reação de redução eletroquímica.
Enquanto o potencial aplicado não for suficiente para desencadear reações de oxiredução, com transferência de elétrons entre o eletrodo e a solução, as superfícies dos eletrodo vão se comportar como se fossem placas de um capacitor, cuja capacitância pode ficar na faixa de 10 a 40 μF/cm2). Por isso essa corrente é também chamada de corrente capacitiva.
Nota
Ou seja, o comportamento da interface eletrodo-solução é análogo ao de um capacitor. E esse é o fundamento físico do fenômeno de “polarização do eletrodo” (Fonte: Electrochemical Methods: Fundamentals and Applications, 2nd Edition, 2000).
O capacitor é um componente eletrônico formado por dois condutores separados por um material isolante chamado de dielétrico. O qual pode ser feito de papel, filme plástico, mica, vidro, cerâmica, ar ou vácuo.
O capacitor pode ser carregado por uma fonte (Figura D.16), e a sua capacidade de armazenamento (capacitância) segue a equação D.33.
Figura D.16. Símbolo de um capacitor e circuito para carregamento. (Fonte: Electrochemical Methods: Fundamentals and Applications, 2nd Edition, 2000)
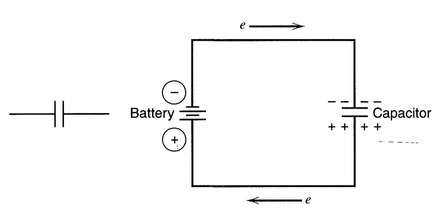
Onde Q é carga elétrica armazenada no capacitor em coulombs (C), E é o pontencial aplicado ao capacitor em volts (V) e C é a capacitância em faraday (F).
Com a aplicação de um potencial nas placas de um capacitor gera uma corrente (não faradaica) com consequente acúmulo de carga conforme a equação D.33. Essa carga acumulada consiste no acúmulo de elétrons em uma placa e uma correspondente deficiência de elétrons na outra placa.
Por exemplo, se os terminais de uma bateria de 2V forem ligados aos terminais de um capacitor de 10 μF será gerada um pico de corrente que decai até zero acumulando uma carga de 20 μC nas placas do capacitor.
Dica
A maioria dos capacitores eletrolíticos possuem polaridade nos terminais e portanto devem ser ligados em uma posição específica no circuito. Enquanto que os capacitores cerâmicos podem ser ligados em qualquer polo.
Também é importante respeitar o limite de tensão suportado pelo capacitor.
Por exemplo, a figura D.17 mostra as variações de corrente e tensão durante o carregamento e o descarregamento de um capacitor em um circuito RC.
Figura D.17. a) Circuito RC em série. Tempo de resposta do circuito quando a chave S está na posição 1 (b) e na posição 2 (c) (Fonte: Skoog, 2002)

Na figura D.17 o gráfico (b), com a chave S na posição 1, ilustra o aumento do potencial no capacitor (vC) durante a acumulação de carga e simultâneamente o pico e queda da corrente de carregamento através do resistor R (iR).
Quanto a chave S é comutada para a posição 2 o capacitor é descarregado e o gráfico (c) mostra o pico no potencial vC seguido de uma queda até o completo descarregamento. Pode-se ver também o pico na corrente de descarregamento (sentido inverso) seguido de queda até 0.
Como já dissemos anteriormente, o comportamento da interface eletrodo-solução é análogo ao comportamento de um capacitor. E portanto, em um dado nível de potencial no eletrodo haverá uma carga elétrica QM no eletrodo metálico e uma carga QS na solução devido à concentração de íons na vizinhança do eletrodo, como mostra a figura D.18
Figura D.18. A interface metal-solução se comportanto como um capacitor com uma carga negativa QM acumulada no eletrodo metálico em (a), e uma carga positiva em (b) (Fonte: Electrochemical Methods: Fundamentals and Applications, 2nd Edition, 2000)
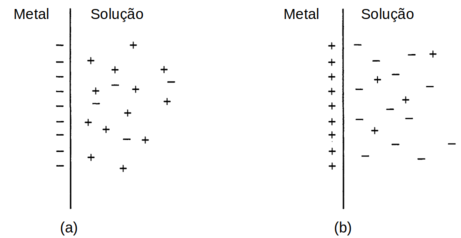
Se a carga do metal é negativa ou positiva em relação à solução depende do potencial na interface e da composição da solução. Em todos os momentos, entretanto, QM = - QS. Lembrar que em uma célula temos que considerar as duas interfaces correspondentes aos dois eletrodos.
A carga no eletrodo metálico (QM) representa um excesso ou deficiência de elétrons e se localiza em uma camada muito fina (< 0,1 Å) na superfície do metal. A carga na solução (QS) é composta por um excesso de cátions ou ânions na vizinhança da superfície do eletrodo.
Ambas as cargas QM QS se distribuem pela área do eletrodo e são expressas como densidades de carga, tais como, σ = QM/A, com a unidade μCcm-2.
Esse conjunto de cargas, íons e dipolos, tanto no metal quanto na solução formam a chamada “dupla camada elétrica”, a qual possui uma capacitância (CD) que pode ficar na faixa de 10 a 40 μCcm-2.
Nota
No entanto, ao contrários dos capacitores reais, cuja capacitância é independente da tensão, a capacitância da dupla camada elétrica é frequentemente função do potencial. (Fonte: Electrochemical Methods: Fundamentals and Applications, 2nd Edition, 2000)
A formação da dupla camada elétrica não é apenas uma “curiosidade”, mas pode ter um efeito significativo na cinética da reação eletroquímica, pois a presença dos íons da dupla camada pode ter um efeito de “blindagem” para os íons mais distantes do eletrodo. E dessa forma reduzem o potencial “percebido” pelas espécies químicas que devem ser oxidadas ou reduzidas mas permanecem mais distantes do eletrodo.
E além disso, na análise de espécies em muito baixas concentrações a corrente não faradaica de carregamento da dupla camada pode ser significativamente maior do que as correntes faradaicas das reações de oxidação ou redução.
As reações em uma célula eletroquímica sofrem efeito de inúmeros fatores como mostra a figura D.19
Figura D.19. Fatores que afetam a velocidade das reações em uma célula eletroquímica (Fonte: Electrochemical Methods: Fundamentals and Applications, 2nd Edition, 2000)
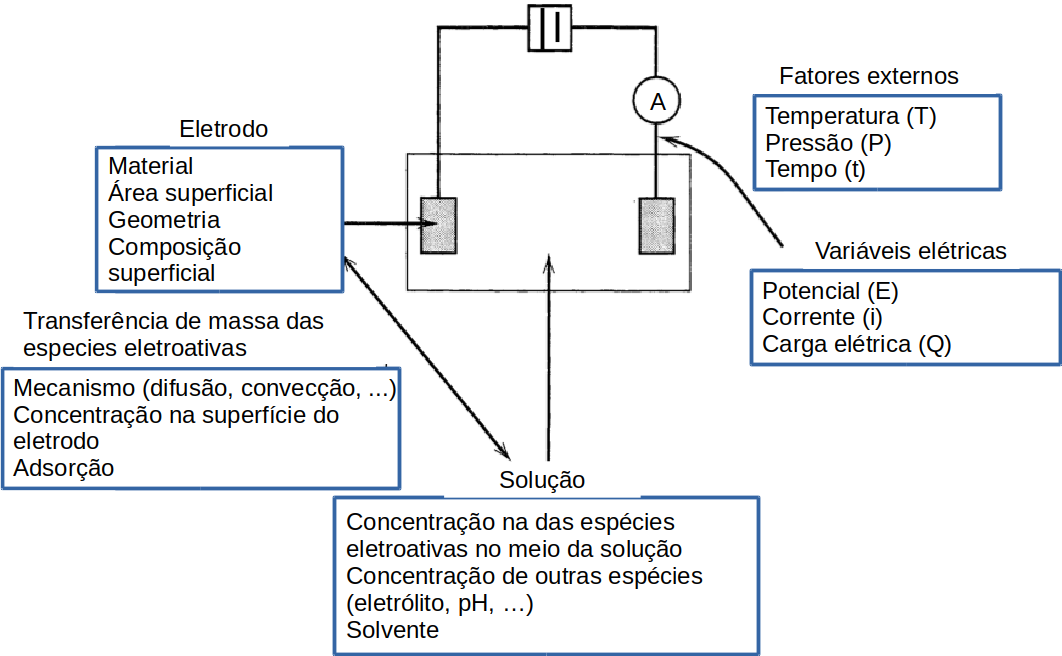
As diferentes técnicas analíticas eletroquímicas manipulam esses diferentes fatores conforme o objetivo. Por exemplo, na Potenciometria a corrente (faradaica) (i) é praticamente nula (i = 0) e o que se deseja analisar é o potencial (E) em função da concentração (C) da espécie eletroativa. Mas como não há passagem de corrente os fatores como área do eletrodo, transferência de massa e geometria do eletrodo, não afetam o potencial diretamente.
Enquanto que na “Voltametria” o que se deseja medir é a corrente (i) em função do potencial aplicado (E) e da concentração (C), mas em condições que estimulam a polarização do eletrodo.
A condução de corrente faradaica em uma célula envolve a ocorrência de uma reação de oxidação, no ânodo, e uma redução, no cátodo. E portanto a intensidade da corrente depende da velocidade de cada reação eletródica.
Por exemplo, qual a velocidade da reação de redução do cádmio (Cd+2 + 2e- → Cd) na célula eletrolítica da figura D.11?
Segundo a Lei de Faraday, a quantidade de produto de uma reação química em um eletrodo é proporcional à corrente segundo a equação D.34
Onde:
N = número de moles do reagente
Q = carga eletrica (C)
n = número de elétrons
F = constante de Faraday = 96485,33 C mol-1
Mas como a corrente é a variação de carga pelo tempo,
A velocidade da reação de eletrólise é proporcional à corrente confome a equação D.36.
No caso da reação de redução do cádmio (Cd+2 + 2e- → Cd), n=2.
Mas como as reações eletrolíticas ocorrem na interface “eletrodo-eletrólito” a velocidade, além de outros fatores cinéticos, depende também da “transferência de massa” do reagente para a superfície do eletrodo e por isso a equação de velocidade costuma ser descrita em função da área (A) do eletrodo conforme a equação D.37.
Onde j é a “densidade de corrente” (A/cm2).
Como já foi visto anteriormente, o desvio do potencial de um eletrodo (E) (ou potencial da célula) do seu valor em equilíbrio (Eeq) com a passagem de corrente (faradaica) é chamado de Polarização.
E o grau de polarização de um eletrodo é medido pela sobrevoltagem ou sobrepotencial (η), que é a diferença entre o potencial do eletrodo real (E) e o potencial termodinâmico ou de equilíbrio (Eeq), conforme a equação D.38.
Um eletrodo “não-polarizável ideal”, é aquele no qual o potencial não muda com a passagem de corrente. Não é o que acontece na prática mas, por exemplo, um eletrodo saturado de calomelano com um poço de mercúrio com grande área, pode se comportar como um eletrodo não-polarizável, em baixas correntes.
Para entender os mecanismos envolvidos no efeito de polarização vamos analisar a figura D.20 que mostra três regiões de uma meia célula onde a polarização pode ocorrer: solução, camada superficial e o eletrodo.
Figura D.20. Etapas de uma reação geral de redução (Ox + ne- ⇆ Red) (Fonte: Electrochemical Methods: Fundamentals and Applications, 2nd Edition, 2000)
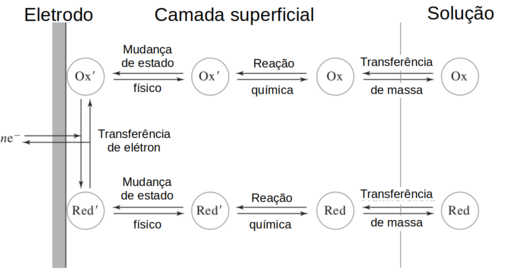
Essas três regiões incluem o próprio eletrodo, um filme superficial adjacente ao eletrodo com apenas algumas moléculas de espessura e o interior da solução.
A figura D.20 ilustra as etapas de uma reação de eletrodo geral (Ox + ne- ⇆ Red), na qual Ox representa a espécie oxidada dissolvida e Red é a forma reduzida também presente na solução.
Como se sabe, a velocidade global de uma reação química composta por direrentes etapas é definida pela etapa “lenta” da reação global. E portanto qualquer estágio intermediário da figura D.20 pode limitar a velocidade da reação global e consequentemente a intensidade da corrente.
E portanto a velocidade da reação eletroquímica, e a correspondente corrente, dependem dos seguintes fatores:
Transferência de massa de Ox para a superfície do eletrodo e/ou de Red da superfície para o interior da solução
Quando uma dessas etapas de transferência de massa é a responsável por limitar a velocidade da reação global, e da corrente, ocorre a chamada polarização de concentração.
Eventuais reações químicas intermediárias antes ou depois da transferência de elétron formando as espécies representadas por Ox' Red'. Essar reações podem ser processos “homogêneos” (Ex: protonação ou dimerização) ou heterogêneos que ocorrem na superfície do eletrodo(Ex: decomposição catalítica).
Quando isso ocorre, os intermediários Ox' ou Red' é que são os verdadeiros participantes do processo de transferência de elétrons.
Se essas reações limitam a velocidade global então ocorre a chamada polarização de reação.
As mudanças de estado físico são resultantes de reações de superfície como adsorção, dessorção ou cristalização, as quais podem também limitar a corrente.
Nesse caso dizemos que se trata de uma polarização de adsorção, dessorção ou cristalização.
E finalmente pode ocorrer a polarização por transferência de carga ou polarização cinética na qual a corrente é limitada pela velocidade de transferência de elétrons do eletrodo para espécies oxidadas no filme superficial (no cátodo), ou de espécies reduzidas para o eletrodo (no ânodo).
Quando é obtida uma corrente em regime permanente (estado estacionário) significa que as velocidades de todas as etapas são iguais. E a intensidade dessa corrente é limitada pela velocidade das etapas mais lentas.
As reações mais simples envolvem apenas a transferência de massa de um reagente para o eletrodo, seguida da transferência heterogênea de elétrons envolvendo espécies não adsorvidas e finalmente a transferência de massa do produto para o interior da solução.
Por isso vamos olhar com mais atenção os dois tipos de polarização que dependem da “transferência de massa” (polarização por concentração), e da “transferência de carga” (polarização por transferência de carga).
A polarização por concentração ocorre quando a velocidade de transferência de massa da solução para a superfície do eletrodo é menor do que a vlocidade de transferência de eletrons de/para o eletrodo. Como resultado a concentração da espécie eletroativa na região da interface eletrodo-solução é menor do que a concentração no meio da solução.
Ou seja, à medida que íons ou moléculas são consumidos pela reação de oxi-redução é necessário o transporte de mais reagente do interior da solução para a interface eletrodo-solução para manter a corrente.
Esse transporte da espécie eletroativa da solução para a superfície do eletrodo, e vice versa, pode ocorrer através de três processos de transporte de massa:
Migração - movimento de íons através da solução causado por atração eletrostática entre os íons e o eletrodo carregado
Difusão - movimento de espécies devido à diferença de concentração ao longo da solução
Convecção - mecanismos de movimento da solução como resultado da agitação ou do fluxo da solução que passa pela superfície do eletrodo
A difusão ocorre quando há uma diferença na concentração de íons ou moléculas entre duas regiões de uma solução. Nesse caso os íons ou as moléculas movem-se a partir da região mais concentrada para a região mais diluída, com uma velocidade que é diretamente proporcional à diferença de concentração.
Por exemplo, na eletrodeposição de íons cádmio sobre um eletrodo de cádmio, como mostra a figura D.21, a concentração dos íons Cd+2 na superfície do eletrodo [Cd+2]0 torna-se menor do que no meio da solução [Cd+2].
Figura D.21. Na figura (a) temos o diagrama esquemático do perfil de distribuição dos íons Cd+2 na camada de difusão e na solução. E na figura (b) temos o gráfico da concentração versus distância que mostra as variações da concentração na superfície do eletrodo de cádmio para diferentes valores de corrente. (Fonte: Skoog, 2002)
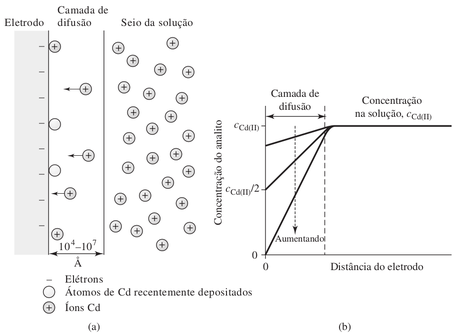
Essa diferença de concentração na superfície e na solução, cria um gradiente de concentração que provoca a difusão dos íons cádmio do meio da solução para a camada próxima da superfície do eletrodo (camada de difusão).
A velocidade de difusão é dada pela equação D.39.
Onde [Cd+2] é a concentração do reagente no meio da solução, [Cd+2]0 é sua concentração de equilíbrio na superfície do eletrodo e k' é uma constante de proporcionalidade ou velocidade.
O valor de [Cd+2]0 pode ser calculado pela equação de Nernst considerando que Ecátodo é o “potencial aplicado ao cátodo” conforme a equação D.40.
Á medida que o potencial aplicado se torna mais negativo, aumentam também a velocidade de difusão e a corrente. Mas a concentração de Cd+2 na superfície ([Cd+2]0) diminui até zero. Nesse ponto é obtida a máxima corrente possível, chamada de “corrente limite”, como mostra o gráfico da figura D.22
Figura D.22. Curva corrente-potencial para uma eletrólise mostrando a região linear ou ôhmica, o início da polarização e o platô da corrente limite. Na região da corrente limite, diz-se que o eletrodo está completamente polarizado, uma vez que seu potencial pode variar amplamente sem afetar a corrente.(Fonte: Skoog, 2002)
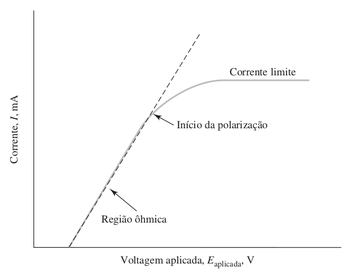
Migração é um mecanismo “eletrostático” no qual os íons se movem sob a influência de um campo elétrico, como mostra a figura D.23
Figura D.23. Migração é o movimento de íons em solução como resultado da atração entre íons e eletrodos de carga oposta, e a repulsão entre íons e eletrodos com carga de mesmo sinal.(Fonte: Skoog, 2002)
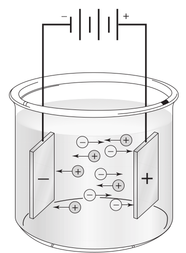
Migração é a principal causa da transferência de massa no interior da solução em uma célula eletrolítica e a velocidade de transferência é diretamente proporcional ao potencial aplicado.
A migração de espécies do analito pode ser indesejável quando, por exemplo, se queira reduzir os ânions em um eletrodo de carga negativa (cátodo) ou oxidar um cátion em um eletrodo de carga positiva (ânodo).
Nesses casos a migração pode ser minimizada pela presença de altas concentrações de um eletrólito inerte chamado de “eletrólito de suporte”. Nesse caso a corrente da célula ocorre pelo deslocamento das cargas do eletrólito de suporte, o qual também contribui para reduzir a resistência da célula, que diminui a “queda ôhmica” (IR).
Na convecção os íons ou moléculas se movimentam na solução devido a processos mecânicos como agitação, vibração, gradientes de temperatura ou de densidade.
A Polarização de Concentração ocorre quando os efeitos de Difusão, Migração e Convecção não são suficientes para transportar um reagente de/para a superfície do eletrodo, com uma velocidade suficiente para produzir uma corrente conforme a equação D.27 (Ecélula = Ecátodo - Eânodo - IR).
E portanto, devido à polarização de concentração é necessário a aplicação de potenciais maiores do que os calculados pela equação D.27, para se obter uma determinada corrente em uma célula eletrolítica.
A Polarização de Concentração é importante em vários métodos eletroanalíticos. Em algumas aplicações, seus efeitos são indesejáveis e existem etapas destinadas à sua eliminação. Em outras, ela é essencial e as condições são ajustadas para garantir sua ocorrência.
As variáveis experimentais que influenciam o grau da Polarização de Concentração são:
concentração do reagente
concentração total do eletrólito
agitação mecânica
tamanho do eletrodo
Na polarização cinética, a grandeza da corrente é limitada pela velocidade de oxidação e/ou redução, em um ou ambos os eletrodos, ou seja, a velocidade de transferência de elétrons não é suficiente rápida para produzir correntes conforme a teoria. Para compensar o efeito da polarização por transferência de carga é necessário aplicar um potencial adicional, ou “sobrevoltagem”.
Normalmente, esse tipo de polarização é minimizado pelo aumento da temperatura e com a diminuição da densidade de corrente (densidade de corrente = corrente por unidade de área do eletrodo - A/m2. Esses efeitos também dependem da composição do eletrodo e são mais pronunciados com metais mais moles, como chumbo, zinco e, especialmente, o mercúrio.
Assim como a queda ôhmica (IR), a polarização por transferência de carga requer a aplicação de voltagens superiores àquelas calculadas para operar uma célula eletrolítica a uma determinada corrente.
A polarização por transferência de carga é mais pronunciada para os processos nos quais o reagente ou o produto de uma célula eletroquímica for um gás, porque a cinética de processos de evolução de gases é complexa e frequentemente lenta.
A alta sobrevoltagem associada à formação de hidrogênio permite a deposição eletrolítica de vários metais que requerem potenciais nos quais seria de se esperar a liberação de H2.